Saúde
Medicamento: Novo transplante de medula óssea pode curar anemia falciforme
Ensaio no Johns Hopkins Kimmel Cancer Center e outros centros descobre que transplante de medula óssea haploidêntico de intensidade reduzida pode curar anemia falciforme
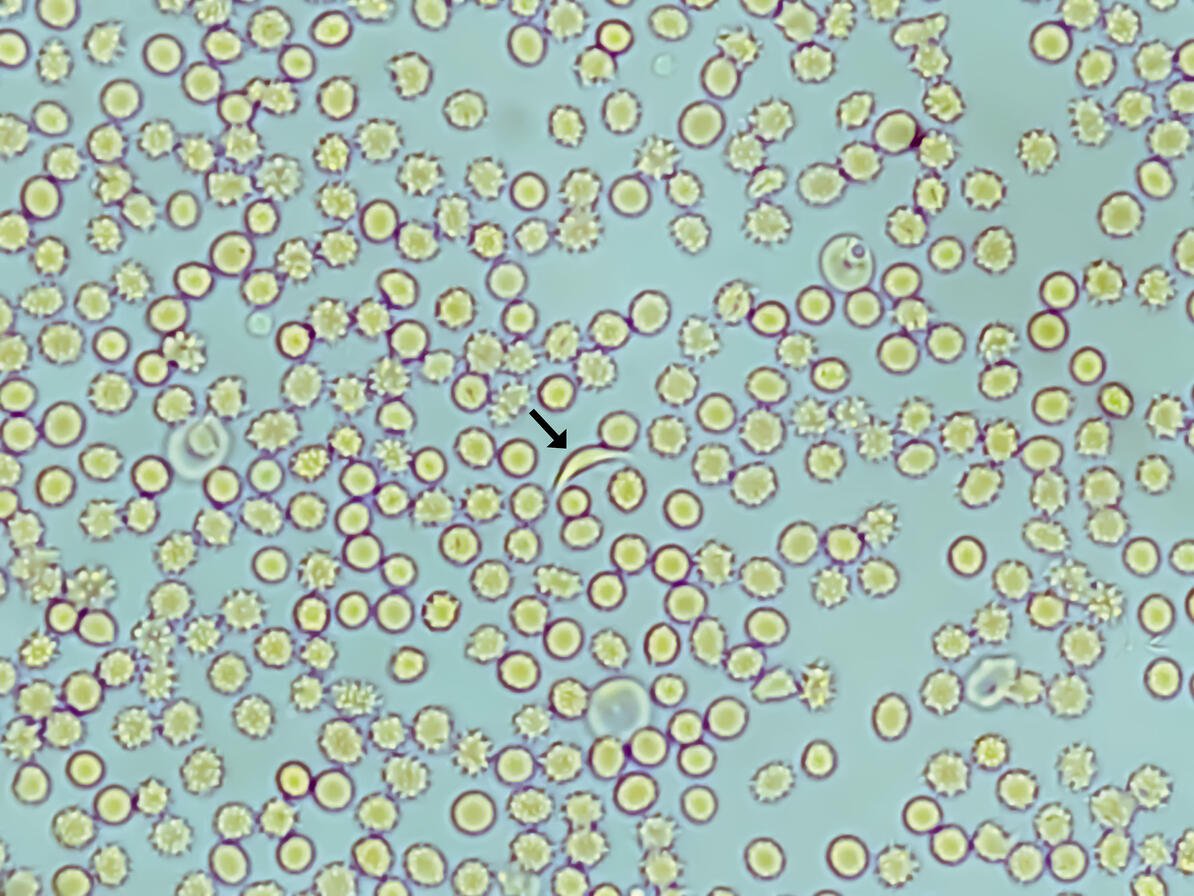
Fotomicrografia de anemia falciforme - Crédito:Md Saiful Islam Khan / Getty Images
Um processo de transplante de medula óssea codesenvolvido por pesquisadores do Johns Hopkins Kimmel Cancer Center é seguro e curativo para adultos com anemia falciforme, de acordo com os resultados de um teste concluído no Johns Hopkins e em cerca de 20 centros de câncer adicionais em todo o país e em Londres. O tratamento, disponível em vários centros médicos dos EUA, é uma alternativa viável e menos custosa aos produtos de terapia genética recentemente aprovados para anemia falciforme, dizem os autores.
Durante esse tipo de transplante, chamado transplante de medula óssea haploidêntico de intensidade reduzida, a medula óssea é doada por um doador "metade compatível", como um pai, irmão, filho, sobrinha, sobrinho, tia, tio ou primo do paciente. Isso significa que as proteínas que ajudam o sistema imunológico do corpo a funcionar, e que estão presentes nas células da medula de um doador, devem corresponder a pelo menos metade dessas proteínas nas células do receptor para serem um bom ajuste e não atacar o corpo do receptor após o transplante.
Antes do transplante, os pacientes são tratados com baixas doses de quimioterapia e recebem irradiação corporal total. Após o transplante, eles recebem ciclofosfamida (um medicamento para prevenir a doença do enxerto contra o hospedeiro, na qual as células imunes na medula do doador atacam seu novo hospedeiro) e outros medicamentos por até um ano.
Das 42 pessoas com anemia falciforme grave que passaram pelo procedimento durante o teste, 95% estavam vivas dois anos após o transplante, e 88% são consideradas curadas e não estão apresentando eventos relacionados à doença. Esses resultados serão publicados na edição de 25 de fevereiro do The New England Journal of Medicine Evidence . Os primeiros resultados foram apresentados em dezembro de 2023 durante a reunião anual da American Society of Hematology.
O estudo mostra uma taxa de enxerto muito alta das células do doador e taxas de cura muito altas, dizem os autores.
"Nossos resultados com transplante alogênico são tão bons quanto ou melhores do que os que você vê com terapia genética", diz Richard Jones , professor de oncologia, diretor do programa de transplante de medula óssea e codiretor do programa de malignidades hematológicas no Kimmel Cancer Center. A maioria das pessoas com anemia falciforme é elegível para o transplante, que custa uma fração do preço da terapia genética, ele diz.
"Muitas pessoas — e talvez a maioria dos adultos — não são elegíveis para terapia genética por causa da exigência de quimioterapia de alta dose que pessoas com danos em órgãos terminais não podem receber", diz Jones. "O risco de efeitos colaterais de longo prazo provavelmente também será maior com a terapia genética, tanto em termos de danos aos órgãos quanto em risco de leucemia."
Um equívoco comum na área médica é que o transplante para anemia falciforme requer um doador perfeitamente compatível e que pode resultar em doença do enxerto contra hospedeiro grave e alta mortalidade, o que este estudo e outros mostraram não ser verdade, diz o coautor do estudo Robert Brodsky , professor de Medicina e Oncologia da Johns Hopkins Family e diretor da Divisão de Hematologia da Faculdade de Medicina da Universidade Johns Hopkins.
O transplante é uma opção muito menos custosa para centros médicos e pacientes, diz Brodsky. Com um transplante, os pacientes ficam no hospital por cerca de oito dias, em oposição a seis a oito semanas para terapia genética. Além disso, "o número médio de transfusões para um paciente de terapia genética é 50, enquanto o número médio de transfusões após um transplante de medula óssea haploidêntico é seis. É feito quase totalmente ambulatorial", diz ele.
Um artigo de revisão comparando transplante de medula óssea alogênico e terapia genética, do qual Jones e Brodsky foram coautores, foi publicado na edição de 25 de fevereiro do periódico Blood Advances . O artigo demonstra que o custo estimado da terapia genética é de US$ 2 milhões a US$ 3 milhões, em comparação com cerca de US$ 467.747 para um transplante.
A idade média dos participantes do ensaio de fase II, que ocorreu de 2017 a 2021, foi de 22 anos; 59% eram homens, 92% eram negros e 4% eram hispânicos. O tempo médio de acompanhamento foi de 37 meses. Efeitos colaterais graves foram incomuns e incluíram três falhas de enxerto, doença do enxerto contra o hospedeiro moderada a grave (22%) e duas mortes no primeiro ano pós-transplante (uma de COVID-19).
A anemia falciforme — um distúrbio sanguíneo doloroso em que os glóbulos vermelhos têm o formato de crescentes em vez de discos e tendem a obstruir os vasos sanguíneos — afeta cerca de 100.000 americanos (principalmente pessoas negras), de acordo com os Centros Federais de Controle e Prevenção de Doenças.
Principais conclusões
- Um novo tratamento, disponível em vários centros médicos dos EUA, é uma opção viável e menos dispendiosa para a anemia falciforme.
- Das 42 pessoas com anemia falciforme grave que passaram pelo procedimento durante o estudo, 95% estavam vivas dois anos após o transplante, e 88% são consideradas curadas e não apresentam nenhum evento relacionado à doença.
- A maioria das pessoas com anemia falciforme são elegíveis para o transplante, que custa uma fração do preço da terapia genética
O ensaio clínico foi apoiado e patrocinado pela Blood and Marrow Transplant Clinical Trials Network; pelos National Institutes of Health; pelo National Heart, Lung and Blood Institute e pelo National Cancer Institute (subvenções U10HL069294 e U24HL138660).
Outros centros que participaram do estudo foram o Vanderbilt University Medical Center em Nashville, Tennessee; a University of California San Francisco School of Medicine; Medical College of Wisconsin em Milwaukee; Northside Hospital em Atlanta; Children's Hospital Colorado; H. Lee Moffitt Cancer Center em Tampa, Flórida; o Roswell Park Comprehensive Cancer Center em Buffalo, Nova York; Atrium Health Levine Children's Hospital em Charlotte, Carolina do Norte; University of Michigan em Ann Arbor; University of Washington em Seattle; Nicklaus Children's Hospital em Miami; Methodist Hospital em San Antonio; University of Alabama em Birmingham; University of Pittsburgh Medical Center; Orlando Health Cancer Institute na Flórida; Children's National Hospital em Washington, DC; St. Mary's Hospital em Londres; Cleveland Clinic; Yale Cancer Center em New Haven, Connecticut; Duke University Medical Center em Durham, Carolina do Norte; e Washington University em St. Louis. Outros autores do estudo foram do Emmes Co. em Rockville, Maryland, e do National Heart, Lung and Blood Institute.



.jpg)
